
来源:《农药》2021年第3期
作者:刘子琪1,2,呼 啸2,袁龙飞1,朱光艳3,李莉1,李薇1,程有普2,陈增龙1(1.中国科学院动物研究所农业虫害鼠害综合治理研究国家重点实验室;2.天津农学院园艺园林学院;3.农业农村部农药检定所)
原标题:新型三唑类杀菌剂氯氟醚菌唑
20世纪70年代三唑类杀菌剂开始投入农业生产,主要通过抑制病原菌细胞膜的C14脱甲基甾醇的合成而导致细胞死亡,对锈病、壳针孢菌和镰刀菌等均具有良好的防治效果,目前主要作用于大豆、果树和蔬菜等农产品。三唑类杀菌剂因其良好的内吸性、预防活性和治疗作用而被广泛使用。据统计,2008年三唑类产品在欧洲的市场份额已超过60%,2018年其在全球的销售额更是高达33.23亿美元。然而,传统三唑类杀菌剂因抗性问题导致防效显著下滑,据2011—2019年的田间测评统计,氟环唑、苯醚甲环唑、戊唑醇和丙环唑对小麦叶枯病菌(Zymoseptoria tritici)的杀菌效果分别从91%、81%、62%、66%下降至36%、56%、23%和24%,其中,氟环唑尤为显著。还有研究指出,戊唑醇对于水生环境以及多种非靶标水生生物的安全存在威胁,并会对其产生长期的负面影响。美国环保署(EPA)也已将烯效唑、己唑醇、戊唑醇、丙环唑和氟环唑传统三唑类杀菌剂列入可能的人类致癌物名单。上述矛盾成为当前三唑类杀菌剂实际应用上的科学难题,导致其面临被禁用的可能,新型三唑类农药的研发与创制是解决该科学难题的有效途径。
氯氟醚菌唑(mefentrifluconazole)是由巴斯夫研发的第1个含异丙醇结构的三唑类杀菌剂,其化学名称为 (2RS)-2-[4-(4-氯苯氧基)-α,α,α-三氟-邻甲苯基]-1-(1H-1,2,4-三唑-1-基)丙-2-醇,商品名为Revysol,CAS号为1417782-03-6,分子式为C18H15ClF3N3O2,相对分子质量为397.8,氯氟醚菌唑的分子结构式见图1。氯氟醚菌唑可溶于水和有机溶剂,在20℃的条件下,水中的溶解度为0. 81 mg/L,其水溶性较低、挥发性较低,不会通过淋溶进入地下水;在有机溶剂丙酮、乙酸乙酯、二甲苯和1,2-二氯乙烷中的溶解度分别为93.2、116.2、8.5、55.3 mg/L。氯氟醚菌唑的熔点为126℃,降解点为300℃,在煮沸状态下会分解,但不易燃烧。氯氟醚菌唑具有较好的生物活性和环境选择性,即便在短期降雨或其他恶劣天气条件下使用后,亦可获得良好的杀菌效果。研究表明,氯氟醚菌唑对哺乳动物、蜜蜂等毒性较低,安全性高,不会造成急性和长期毒性,打破了传统三唑类杀菌剂对人体和动物的潜在危害。目前,氯氟醚菌唑已在韩国、欧盟、澳大利亚、加拿大、美国、中国等全球多个国家和组织展开登记,成为三唑类杀菌剂的重要新生力量。
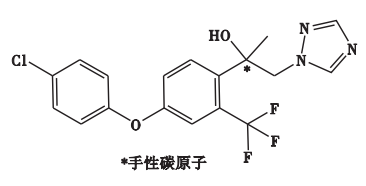
图1 氯氟醚菌唑分子结构式
本文综合国内外相关研究进展,主要从化学合成、生物活性、生态毒性、环境行为以及代谢特征5个方面对新型三唑类杀菌剂氯氟醚菌唑进行综述,旨在为其农业合理应用、科学有效管理与生态风险规避提供理论支撑。
1 氯氟醚菌唑的化学合成
目前氯氟醚菌唑的合成方法主要是化学合成,现主要存在2种总收率高、合成工艺较短、适合工业生产的合成路线。合成路线Ⅰ是以2-溴-5-氟-三氟甲苯为起始原料经醚化、酰化、环氧化和开环取代4步反应得到目标产物,总收率高达92%,化学反应方程式见图2;合成路线Ⅱ是由4-氟-2-三氟甲基苯乙酮和4-氯苯酚为起始原料在碱性条件下经取代、环氧化、开环3步反应得到氯氟醚菌唑原药,总收率可达75%(见图2)。
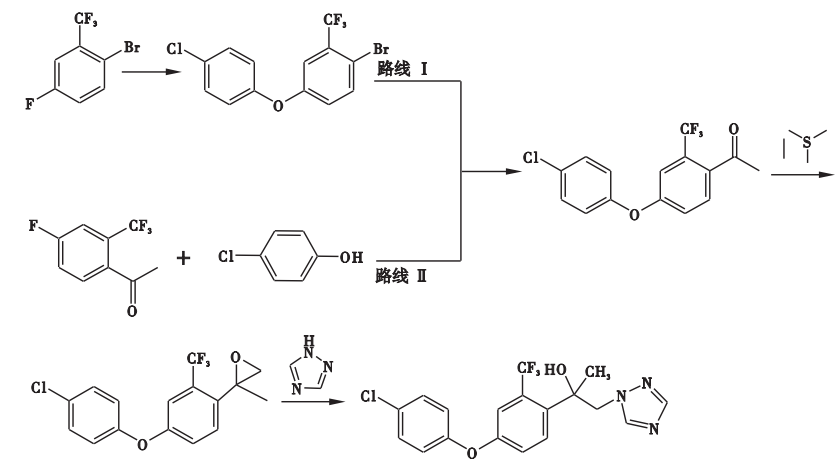
图2 氯氟醚菌唑的合成路线
上述2种合成路线中,氯氟醚菌唑的总收率都超过75%,其中合成路线Ⅰ的总收率高达92%,而合成路线Ⅱ具有合成工艺路线短、反应条件温和、原材料易获得等优点,体现出更强的工业化规模生产的价值。同时,值得注意的是氯氟醚菌唑化学结构中含有手性碳原子(见图1),包含2个对映异构体,这在后续的毒理学评价、环境行为特征,以及手性单体农药不对称合成研究中需要重点关注。
2 氯氟醚菌唑的生物活性
生物活性是评价氯氟醚菌唑杀菌功效的关键。氯氟醚菌唑属于甾醇脱甲基抑制剂类,通过阻止麦角甾醇的生物合成,改变真菌细胞质膜的结构和功能,从而抑制细胞生长。研究表明,氯氟醚菌唑高效的杀菌活性与其分子中独特的异丙醇结构密切相关,它能够很好地抑制壳针孢菌的菌株转移,减少病菌突变,对多种抗性菌株体现出高效性。相对于传统三唑类杀菌剂,氯氟醚菌唑具有更高的选择性和内吸传导性,适用于世界范围内60多种大田、经济和特种作物,尤其对于谷物病害,如小麦叶枯病、锈病、大麦叶斑病以及亚洲地区常见的水稻纹枯病和稻瘟病,乃至真菌病害均具有优异的生物活性。通过活体盆栽的方法测定氯氟醚菌唑对黄瓜炭疽病(Colletotrichum orbiculare)、玉米锈病(Puccinia sorghi Schw)以及小麦白粉病(Blumeria graminis Speer)的杀菌活性,结果表明,氯氟醚菌唑对这3种病害均具有一定的杀菌活性。在1.56 mg/L质量浓度下,氯氟醚菌唑对小麦白粉病的盆栽杀菌活性可达100%,在0.39、0.1 mg/L质量浓度下,氯氟醚菌唑的防效也均优于对照药剂丙环唑和烯肟菌胺;氯氟醚菌唑对玉米锈病的盆栽杀菌活性在25~100 mg/L的质量浓度下可达100%,而在6.25 mg/L的质量浓度下,氯氟醚菌唑的杀菌活性优于对照药剂丙环唑,但低于对照药剂吡唑醚菌酯;氯氟醚菌唑对黄瓜炭疽病的盆栽杀菌活性则低于对照药剂咪鲜胺和嘧菌酯。可见,在测试质量浓度下氯氟醚菌唑对小麦白粉病防效优异,对黄瓜炭疽病、玉米锈病防效中等。目前,已有研究证实,传统三唑类杀菌剂对小麦叶枯病菌、小麦壳针孢菌(Sphaeropsicaceae)等靶标病害的防效已出现显著下降,而氯氟醚菌唑作为新型脱甲基抑制剂类杀菌剂对此类病害具有良好的防效。根据2017—2019年田间测评结果证实,其对小麦叶枯病菌的防治效果从86%升至94%,且病害未出现明显抗药性。这也进一步说明氯氟醚菌唑防效优异,是传统三唑类杀菌剂抗性管理的有效替代品种。
3 氯氟醚菌唑的生态毒性
氯氟醚菌唑对非靶标生物的生态毒性是评定其风险等级的重要指标。国际纯粹与应用化学联合会(IUPAC)指出,氯氟醚菌唑对哺乳动物的急性毒性和长期(生殖)风险较低。通过大鼠和兔子的急性毒性毒性研究发现,氯氟醚菌唑的急性经口毒性LD50>2,000 mg/kg、急性皮肤毒性LD50为5,000 mg/kg b.w.、急性吸入毒性LC50>5.31 mg/L。通过对小鼠和家兔的毒性研究,氯氟醚菌唑的每日可允许摄入量(ADI)被设定为0.035 mg/(kg·b.w.·d),急性参考剂量(ARfD)为0.15 mg/kg b.w.。对小鼠和狗进行了长期重复剂量毒性和致癌性研究发现,当氯氟醚菌唑通过口服、吸入或经皮肤等途径进入体内时,主要的靶标器官是肝脏,并观察到低等急性毒性与非致癌性,不会引起生殖细胞损伤和幼崽性别转化的现象。通过怀孕的大鼠和兔子测定氯氟醚菌唑对哺乳动物产前发育毒性影响,结果表明,对母体用药不会引起胎儿的不良反应,对于胎儿的生长发育、妊娠期长度以及后代的存活率也不会产生影响,这说明氯氟醚菌唑对怀孕的大鼠和兔子既无胚胎毒性,也无致畸性。
在室内和田间条件下,氯氟醚菌唑对蜜蜂暴露风险评估指出,其对意大利蜜蜂和大黄蜂低毒,对意大利蜜蜂的急性经口和急性接触毒性LD50均为>100 μg/只,对大黄蜂的急性经口毒性LD50>195.4 μg/只,急性接触毒性LD50>200 μg/只。氯氟醚菌唑对山齿鹑具有中度急性毒性,LD50为816 mg/kg;其对水生生物(藻类、溞类、鱼类)也具有中度急性毒性,例如,氯氟醚菌唑对浮萍的7 d急性毒性EC50为2.02 mg/L,对月牙藻72 h急性毒性EC50和96 h慢性最大无作用浓度NOEC分别为1.352、0.103 mg/L;对大型溞的48 h急性毒性 EC50和21 d慢性最大无作用浓度NOEC分别为0.944、0.016 mg/L;对虹鳟鱼96 h急性致死中浓度LC50为0.532 mg/L。相比于传统三唑类杀菌剂,氯氟醚菌唑对于生态环境的风险更低。
4 氯氟醚菌唑的环境行为
痕量追踪生态环境介质中氯氟醚菌唑及其代谢物,是其生态环境安全评价的基础。目前已有研究通过超高效液相色谱-串联质谱(UHPLC-MS/MS)技术结合多壁碳纳米管(MWCNTs)建立了动植物源食品中氯氟醚菌唑的分析方法。氯氟醚菌唑在水体中的耗散动力学研究指出,在富含天然沉积物的水体中,氯氟醚菌唑表现出较高的持久性,DT50为163.2 d,主要的残留物为其代谢产物1,2,4-三氮唑和4-[2-羟基-1-(1H-1,2,4-三唑-1-基)丙-2-基]-3-(三氟甲基)苯酚。而在水体中其DT50仅为7.2 d,说明水体中氯氟醚菌唑的降解速度明显快于富含沉积物水体中的降解速度。通过三唑类和氯苯标记的氯氟醚菌唑在无菌水中辐照,形成主要的光降解产物为4-{4-[2-羟基-1-(1H-1,2,4-三唑-1-基)丙-2-基]-3-(三氟甲基)苯氧基}苯酚、6-(4-氯苯氧基)-3-甲基-3-(1H-1,2,4-三唑-1-基甲基)-2-苯并呋喃-1(3H)-酮、6-(4-羟基苯氧基)-3-甲基-3-(1H-1,2,4-三唑-1-基甲基)-2-苯并呋喃-1(3H)-酮。氯氟醚菌唑在室内土壤中的降解规律表明,其在好氧条件下表现出较高的持久性,DT50为268 d,无主要代谢物生成;在厌氧条件下,氯氟醚菌唑降解缓慢,降解途径与好氧条件下相似,也未检测到主要代谢产物;氯氟醚菌唑在土壤中表现出轻微的迁移性,且其吸附性与pH值无关。在大田环境下,氯氟醚菌唑在土壤中DT50为200 d,半衰期相比室内条件下略短。欧盟评估报告中同样证实了这一点,室内条件下,氯氟醚菌唑DT50范围为104~477 d,而大田中其DT50范围为96.5~611 d。
5 氯氟醚菌唑的代谢特征
明确氯氟醚菌唑在动植物体内的代谢特征对其暴露风险评估至关重要。研究发现,氯氟醚菌唑在大豆、小麦壳、葡萄藤和葡萄中残留主要成分为母体,而在小麦籽粒和大豆种子中,氯氟醚菌唑的残留量极低,其主要残留是三唑类衍生代谢物(TDM),其中以三唑丙氨酸为主。在对叶菜类蔬菜、块根类蔬菜和谷类作物的代谢研究中发现氯氟醚菌唑和TDM为主要残留物。北欧和南欧通过对小麦、萝卜、胡萝卜、花椰菜、西兰花、莴苣和菠菜中氯氟醚菌唑的残留检测发现,7种检测样品中的氯氟醚菌唑含量较低,没有高于残留的定量限。在模拟食品加工条件的水解研究中发现,氯氟醚菌唑和TDM的残留量保持稳定。
氯氟醚菌唑在山羊、家禽和鱼类体内的代谢特征研究指出,其在山羊和家禽体内表现出基本一致的代谢途径,但存在着不同的结合反应和转化率。在山羊体内,氯氟醚菌唑及其代谢物1,2,4-三氮唑是残留的主要成分,其次代谢物2-[4-(4-氯苯氧基)-2-(三氟甲基)苯基]丙烷-1,2-二醇的含量较低;而在家禽体内,2-[4-(4-氯苯氧基)-2-(三氟甲基)苯基]丙烷-1,2-二醇是残留的主要成分,未经修饰的氯氟醚菌唑和1,2,4-三氮唑含量也较高;鱼体内的主要残留物质为氯氟醚菌唑和1,2,4-三氮唑,与山羊体内残留物质相似。上述研究为动植物体内氯氟醚菌唑暴露风险评估以及残留定义的确定提供了科学依据。
6 发展与展望
氯氟醚菌唑作为首个异丙醇三唑类杀菌剂,弥补了传统三唑类杀菌剂日益增强的抗药性和生态环境风险高的缺点,成为传统三唑类杀菌剂有效的替代品种,应用前景广阔。同时,值得注意的是,氯氟醚菌唑属于手性三唑类杀菌剂,2个对映体虽然具有相同的理化属性,但极有可能体现出不同的选择性差异,包括活性、毒性、降解、代谢等,已有研究通过超高效液相色谱串联质谱开发了氯氟醚菌唑对映体的手性分离分析方法;欧盟的评估报告也指出,R-氯氟醚菌唑和S-氯氟醚菌唑在植株、土壤和水体的降解过程中比例保持不变,没有优先代谢或吸收,但在哺乳动物山羊和大鼠体内发现S-氯氟醚菌唑优先代谢,且相比R-氯氟醚菌唑更具毒理学活性。目前针对氯氟醚菌唑的研究尚且集中在外消旋体层面,对映体层面选择性生物活性、生态毒性以及环境行为的差异仍不清晰,因此,从对映体水平研究氯氟醚菌唑的立体选择性差异将是未来研究的重点方向。
(1)本网旨在传播信息,促进交流,多方面了解农药发展动态,但不构成任何投资建议。
(2)所有文章仅代表作者观点,不代表本网立场。
(3)“信息来源:江苏省农药协会 农药资讯网”为原创文章,转载时请注明来源和作者。
(4)本网转载文章及图片的版权属于原作者,若有侵权,请联系删除。