
1 固体分散技术
1.1 固体分散技术的概念
固体分散技术是将药物高度分散于惰性材料载体中,形成的一种以分子、无定形或微晶化状态存粉碎、筛分散体系。利用固体分散技术制备的剂型称为固体分散体,亦称为固体分散物、固态均质体或均一体。固体分散技术始于医药领域,研究表明,将难溶性药物在水溶性载体中形成分子分散体系,可以改善药物的溶解性能,加快溶出速度,提高生物利用度。1933年丹麦Ferrossam制药公司首次以脂溶性的氢化植物油为基质,稀乙醇为冷却剂制备维生素AD滴丸。1956年Bjornssion等开始用水溶性的聚乙二醇4000为基质,植物油为冷却剂制备苯巴比妥滴丸。但大多数学者仍认为固体分散技术是20世纪60年代由Sekiguchi制备磺胺噻唑(ST)/尿素固体分散体开始逐渐发展起来的一种新技术。
Sekiguchi等在1961年首次提出固体分散体(Solid dispersions,SD)概念,以尿素为载体,用熔融法制备了磺胺噻唑固体分散体,使难溶性药物的溶解度与溶出速率得到了明显改善。此后,固体分散体的相关研究和应用不断获得拓展。20世纪80年代以来,通常采用水溶性和强亲水性的材料作为固体分散体载体,以增加一些难溶性药物的溶解度和溶出速率,提高药物口服后的生物利用度。
近年来,固体分散技术已从增加药物的溶解性能,提高生物利用度进入到缓(控)释和靶位释药研究。人们采用难溶性材料如脂溶性、脂质材料等为载体制备具有缓释或控释功能的固体分散体来控制药物的释放,以达到缓释或控释的目的,大大扩展了固体分散技术的应用范畴。该转变为固体分散技术在农药制剂中的应用提供了广阔应用前景,日益受到农药制剂开发者的重视。
1.2 固体分散技术原理
固体分散技术与简单的机械物理混合有本质上的区别,该技术是利用熔融法、溶剂法、喷雾干燥法等物理化学方法使药物形成熔融态、溶液态、微乳态、乳状液态,经干燥处理后,药物以分子、无定形或微晶化状态等形式与载体均匀混合的固体分散体系。本质上,乳化-溶剂挥发法,乳化(微乳化、溶解)-喷雾干燥法,复凝聚法等方法均属于固体分散技术,最终干燥所得的物料颗粒粒径为微米级的称为微球剂,大于100μm的颗粒粒径归于颗粒剂 [包埋(缓释)颗粒剂或缓释颗粒剂] 的范畴。
1.3 药物在固体分散体中的分散状态
药物在载体中分散的状态分为低共熔混合物、固态溶液、无定形固体及分子包合物等。
1.3.1 低共熔混合物
2种或2种以上药物混合后,出现润湿或液化现象的混合物,其混合形成最低熔点的混合物称为低共熔混合物。低共熔混合物的熔点称为低共熔点。如将45 g熔点为179℃的樟脑与55 g熔点为42℃的水杨酸苯酯熔融混合后,其熔点仅为6℃。
在低共熔混合物中,药物是以超细结晶状态分散于固态载体中,是一种物理混合物,在X射线粉末衍射图中,药物衍射峰仍然存在,在扫描电镜下可见药物结晶,而在差热分析(DTA)图中,有效成分熔融峰随载体比例的增加,会逐渐消失,表明形成了低共熔混合物。
1.3.2 固态溶液
固态溶液,顾名思义就是一种固体状态的“溶液”,在常温下呈“固态”而不是“液态”。在熔融状态下,将一种固体熔解在另一种固体中,形成一种分散均匀的熔液,冷却、降温固化成均匀的固体,如不锈钢就是由不同比例铁、镍、铬组成的固态溶液。固态溶液与传统意义上的溶液本质上一样,属于分子水平上的分散,只不过一个可以自由流动,一个不能流动;一个分子间距离较大,一个分子间距离较小。
按药物和载体材料的互熔情况,可分为完全互熔与部分互熔,按晶体结构可分为置换型与填充型。如果药物与载体分子的大小很接近,则一种分子可以替换另一种分子进入其晶格结构产生置换型固态溶液,这种条件下,药物与载体在任何比例下都能形成固态溶液,故又称为完全互熔固态溶液;而当药物与载体分子大小差异较大时,则一种分子只能填充进入另一分子的晶格结构的空隙中形成填充型固态溶液,这种溶液只能在特定的药物载体组成比例下形成,故又称为部分互熔固态溶液。
固态溶液是一均相体系,在X射线粉末衍射图上,药物结晶衍射峰消失,扫描电镜下无药物结晶出现,且DTA图上药物熔融峰消失。如聚乙二醇是一类用于制备难溶性药物固体分散体优良的基质,其特点是有机药物的相对分子质量大多小于400或500,而聚乙二醇相对分子质量为1,500、4,000和6,000,因而可形成填充型固态溶液。将聚乙二醇/药物熔解后迅速冷却,使药物难于形成晶核,由于低温时介质黏度较大,固化时间很短,故溶质仅可形成微晶。
当形成的固态溶液外观透明时,称为玻璃态固态溶液。
1.3.3 无定形固体
无定形固体指药物以无定形态分散于载体中。无定形固体内部原子或分子排列无周期性,如同液体那样杂乱无章地分布,可看作过冷液体,如玻璃、松香、明胶等。无定形固体有如下通性:宏观性质具有均匀性,这种均匀性来源于原子无序分布的统计性规律;物理性质一般不随测定方向而变,称为各向同性;不能自发地形成多面体外形;无固定的熔点;由于无周期性结构,不能对X射线产生衍射效应。一般药物与载体以溶液态、微乳液态、乳状液态混合后,固化后药物均以无定形状态分散于载体中。
1.3.4 分子包合物
分子包合物是一类有机晶体。其结构中含有2种结构单元,所以包合物是由2种化合物组成:一种是能将其他化合物包埋在它的结构骨架空穴里的化合物,称为包合剂或主体分子;另一种是被包埋在包合剂结构的空穴或孔道中的化合物,称为被包合剂或客体分子。客体分子的大小受包合剂空穴的几何尺寸及形状的限制。包合物的组成(包合剂与被包合剂的比例)由骨架中可利用的空隙数决定。20世纪40年代H.M.鲍威尔利用X射线衍射法探明了包合物中主体分子与客体分子之间通常不会形成很强的化学键,包合物中主、客体分子原有的化学性质不变,大多数包合物中主体分子与客体分子之间以范德华力或氢键相结合。
包合物可分为结晶包合物、分子包合物(如β-环糊精包合物)及大分子包合物(如分子筛)等。
1.4 固体分散技术的特点
固体分散技术是一种制剂制备的新型技术,利用不同性质的载体及制备技术,既可以提高制剂的速释性,也可以延缓制剂的缓释性。该技术有其独特的特点:
⑴ 将难溶性药物制备成固体分散体,药物以分子、无定形或微晶化状态分散于水溶性载体中,改善了药物的溶解度,提高了生物利用度。
⑵ 将易挥发、易分解的不稳定药物制备成固体分散体系,可以增加药物的稳定性,减少用药剂量,减轻药物的不良反应。
⑶ 以肠溶性材料为载体,通过固体分散技术将药物与肠包衣材料制备成固体分散体,使药物在胃的酸性环境下几乎不溶,而在肠道中易溶,从而使药物在胃里不释放而在肠道中释放,达到控释目的。
⑷ 以不同的载体制备同一药物的固体分散体,其溶出度亦不同。用可溶性载体制备,则提高在体内的释放速率;用难溶性载体制备,则减缓在体内的释放速率,从而可制备成速释型或缓释型制剂。
1.5 固体分散体及载体的分类
固体分散体按释放性能分为速释型(速效型)固体分散体、缓释型固体分散体和靶向释药型固体分散体。它们相应的载体分别为水溶性载体、难溶性载体及肠溶性载体,由于释放速度不同,其采用的载体也不同。
1.5.1 速释型固体分散体及载体
速释型固体分散体就是利用亲水性载体制备的固体分散体系,大多数的固体分散体属于这一类型(对于医药领域而言)。
对于难溶性药物,利用水溶性载体制备的固体分散体,不仅可以保持药物的高度分散状态,而且对药物具有良好的润湿性。对提高药物溶解度,加快药物溶出速率,从而提高药物的生物利用度方面具有重要的意义。如采用熔融法,以PEG 6000为载体,制成灰黄霉素滴丸,结果表明,固体分散体口服在2 h内几乎完全被吸收,而微粉片30~80 h内仅吸收44.3%,药物/载体比1∶10~1∶5的灰黄霉素分散体在人体内的吸收量比微粉片高1倍多。
水溶性载体主要用于改善难溶性药物的生物利用度,故速释型固体分散体所用的载体多为水溶性的高分子化合物、有机酸及糖类等。常用于增溶作用的水溶性聚合物,如聚乙烯吡咯烷酮(PVP)、聚乙二醇(PEG)等;水溶性小分子化合物,如糖类物质蔗糖、葡萄糖等,有机酸类物质枸橼酸、酒石酸、琥珀酸等,醇类如甘露糖醇、木糖醇、山梨醇、半乳糖等;其他亲水性辅料,如改性淀粉、微晶纤维素等。近年来,对水溶性固体分散载体的研究出现了由单一载体向复合载体及添加表面活性剂的载体方向发展趋势。
1.5.2 缓(控)释型固体分散体及载体
缓(控)释型固体分散体是指以难溶性或脂溶性载体制备的固体分散体。该分散体可以看作溶解扩散或骨架扩散体系,释放机理与相应的缓释制剂和控释制剂相同,释放符合一级动力学方程、Higuchi方程和零级动力学方程。Nagib等以乙基纤维素为载体,用溶剂法制备了磺胺嘧啶的固体分散体,体外溶出试验结果表明,该固体分散体释药过程的动力学是表观零级动力学方程和控制扩散。
缓(控)释型固体分散体常用的载体主要有甲基纤维素(MC)、乙基纤维素(EC)、邻苯二甲酸醋酸纤维素(CAP)、羟丙基甲基纤维素(HPMC)、羟甲基乙基纤维素(CMEC),脂质材料如胆固醇、β-谷甾醇、棕榈酸甘油酯、蓖麻油蜡等。
1.5.3 肠溶型固体分散体及载体
肠溶型固体分散体就是以肠溶性材料为载体,制备的靶向于肠道溶解释放药物的固体分散体。传统的固体分散体的研究绝大多数都是以水溶性载体如聚乙二醇(PEG)、聚乙烯吡咯烷酮(PVP)等促进难溶性药物迅速溶解释放而制备的固体分散体,在促进药物释放和提高生物利用度方面卓有成效。近年来随着药剂学的发展和新辅料的出现,已经逐渐出现了一些肠溶固体分散体的研究。例如硝苯吡啶肠溶固体分散体的制备,硝苯吡啶为难溶性药物,生物利用度低,Hasegawa将硝苯吡啶与乙醇/氯甲烷混合溶剂溶解后,用喷雾器喷于蔗糖表面,制成肠溶固体分散体,体外溶出试验表明,该固体分散体在胃液中溶出极少(50 min内少于0.4 mg/L),而在pH5.8的肠液中释放却大大加快(30 min时达到60 mg/L)。
以水溶性材料(PEG-6000)和肠溶性材料(聚丙烯酸树脂)为复合载体制备的固体分散体,能够改善许多难溶性药物的生物利用度,且具有缓释性,有效解决了以往利用控制溶解来制备难溶性药物的缓释制剂而导致的生物利用度较差的问题,为缓释制剂的开发提供了一条新的途径。
肠溶性固体分散体常用的载体有邻苯二甲酸羟丙基甲基纤维素(HP-55)、邻苯二甲酸醋酸纤维素(CAP)、羧甲基乙基纤维素(CMEC)、含季铵基团的聚丙烯酸树脂类等。
1.6 固体分散体的制备方法
固体分散体常用的制备方法有熔融法、溶剂法(共沉淀法)、溶剂-熔融法以及喷雾干燥法等。
1.6.1 熔融法
熔融法是将药物与载体混匀,用水浴或油浴加热至熔融或先将载体加热至熔融后,再加入药物,使药物熔解在液态载体中,迅速冷却成固态溶液的制备方法,适合于熔点较低的载体,如聚乙二醇等。在较低的温度下,使熔融态的载体可以融化高熔点的药物,2者相容,均匀混合,使之形成均匀的固体分散体(固态溶液)。该方法简便且经济,适用于对热稳定的药物。但需要考虑药物与载体的互熔问题。
1.6.2 溶剂法
溶剂法也称共沉淀法,是将药物和载体同时溶于同一溶剂中,或者将药物和载体分别溶于相同的溶剂后混合均匀,除去溶剂而得固体分散体。该方法适合于载体熔点较高或药物对热不稳定及易挥发药物,常用的溶剂有氯仿、二氯甲烷、乙醇、丙酮等易挥发的溶剂。该法与微球剂的制备方法——溶剂挥发法类似。
1.6.3 溶剂-熔融法
溶剂-熔融法是将药物用少量的有机溶剂溶解后与熔化的载体混合均匀,除去溶剂或不除去溶剂,冷却固化而得固体分散体。该方法适合于某些液体药物,或受热稳定性较差的小剂量药物。
1.6.4 喷雾干燥法
喷雾干燥的原理:通过压力式或气流式雾化器将含有药物与载体均匀混合而成的液体物料通过高速(压缩)气流使液体雾化成微小的液滴,这种极小的液滴在喷入到热风(适用于O/W乳液)或含有惰性气体(如氮气,适用于纯有机溶剂)的热气流时,液滴中的水分或溶剂会瞬间蒸发而固化成微粒,最后收集粉末即可(图1)。
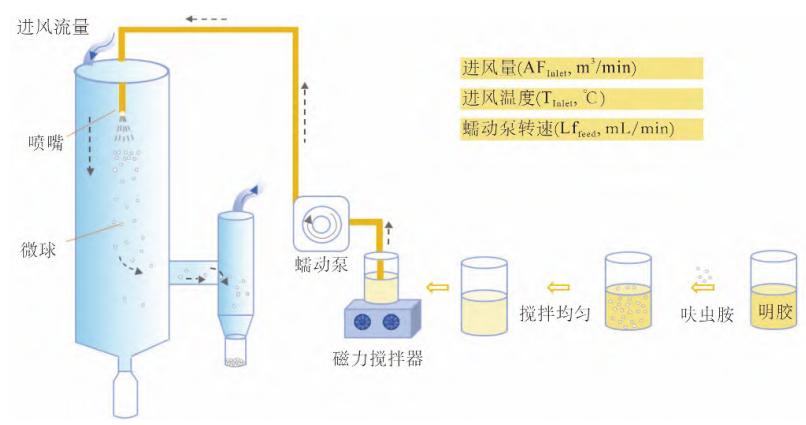
图1 喷雾干燥法工艺示意图
该方法既适用于油溶性聚合物载体如聚乳酸、聚乳酸-乙醇酸共聚物,也适用于水溶性聚合物载体如壳聚糖、明胶、海藻酸钠等。油溶性载体与非极性药物可通过乳化-溶剂挥发法制备O/W乳状液;非极性药物与水溶性聚合物载体可通过乳化、微乳化的方法制备O/W乳状液或微乳液,即先将药物溶解于少量的有机溶剂中成为油相,在乳化剂的作用下,加入水溶性载体水溶液中经过搅拌形成O/W乳状液或微乳液;极性药物直接溶解于水溶性载体中形成水溶液。上述溶液、乳状液及微乳液等经过喷雾干燥机喷雾干燥,收集其喷出的粉末即得到固体分散体(微球剂)。
1.6.5 复凝聚法
复凝聚法(Complex coacervation)是一种相分离过程,相分离过程就是凝聚过程,故也称为凝聚法。该法在制药上的应用主要是水相分离法,其凝聚是在水溶液中进行的,所以药物是非水溶性的固体或液体。即由2种或多种带相反电荷的高分子聚合物作为复合载体,将药物分散在高分子聚合物水溶液中,介质的改变(pH、温度、浓度、电解质等)使聚合电解质同时去溶剂化,导致带相反电荷的高分子聚合物发生静电作用,相反电荷的高分子聚合物相互吸引后,聚合物在水溶液中的溶解度降低并产生液-液相分离,与药物共同凝聚成球。经常使用的2种带相反电荷的高分子聚合物组合:明胶-阿拉伯胶、海藻酸钠-壳聚糖、海藻酸钠-聚赖氨酸、明胶-羧甲基纤维素等。复凝聚法工艺示意图见图2。

图2 复凝聚法工艺示意图
1.6.6 其他新型的固体分散技术
固体分散技术自1961年被提出以来,溶剂法、熔融法等传统制备技术得到了长足的发展。溶剂法需要用溶剂来溶解药物和载体,再通过除去溶剂得到固体分散体,此法需要消耗较多的有机溶剂,不但成本高昂且污染环境;采用熔融法制备固体分散体时,需要在高温条件下先把载体融化后再加入药物混匀,此法只适用于热稳定性的药物和材料。因此,亟待开发新型的固体分散技术,寻求高效无污染的方法制备性能更佳的固体分散体越来越引起研究者们的重视。近年来,超临界流体技术、热熔挤出技术、微波淬冷技术等新型技术也逐步发展并应用于固体分散体的制备。
⑴ 超临界流体技术
利用二氧化碳价廉易得、无毒无污染、超临界条件易于实现等特点,通常把二氧化碳作为流体使用。超临界二氧化碳适宜的临界温度和惰性气体性质可避免热敏性及易氧化物质的破坏,同时渗透性高、黏度低、表面张力低及可循环利用,省时增效。超临界流体技术具有传统方法无可比拟的优势,所制备的固体分散体纯度高、粒径均匀可控、无溶剂残留等,但因为大多数难溶性药物在二氧化碳中的溶解度较小,且随着药物或载体材料的极性变大,溶解度将更低,所以采用该技术制备固体分散体目前并未得到广泛应用。
⑵ 热熔挤出技术
热熔挤出技术(Hot melt extrusion,HME)最初是一种应用于塑料工业、饲料生产、食品加工等工业化的大生产技术,于20世纪70年代引入到制药行业后得到飞速发展,尤其是在改善难溶性药物溶出度方面取得了显著的成效。热熔挤出技术是指将多相状态的物料在适宜的温度下熔化或软化,在强烈剪切与混合的作用下,不断减小粒径,同时彼此进行空间位置的对称性交换与渗透,最终使物料呈单相状态并高度均匀分散于载体中的新技术。热熔挤出技术无需溶剂参与,可持续操作,操作步骤少,并能提高药物的生物利用度,但该法不适用于热不稳定、高熔点、不耐剪切的药物和载体材料。
⑶ 微波淬冷技术
微波技术是一种独特的技术,它从物质内部开始整体均匀地进行加热。在制备固体分散体的过程中,微波加热将药物熔化并快速通入液氮,使之立刻淬冷,药物的内部结构还来不及重新排列或发生结晶,这样使晶态药物无定形化。微波淬冷技术是将药物与载体的混合物放置于微波炉中熔融,待完全熔融后,趁热取出,快速用液氮(−196℃)淬冷使其固化,干燥后使其粉末化。微波淬冷技术使药物经历了从熔融到淬冷的极速过程,相比之下,其内部药物无定形状态比其他制备技术无序度更高、所维持的时间更长,这是造成其溶出与溶解度增大的重要原因。此外,采用微波辐射加热制备固体分散体具有加热过程中无需使用有机溶剂,热源可循、节能,非接触加热、安全性高,可改变药物晶态等特点。
2 利用固体分散技术制备的农药新剂型——包埋(缓释)颗粒剂
包埋(缓释)颗粒剂是以高分子聚合物作为载体,利用固体分散技术原理,农药有效成分以分子、胶体、无定形或微晶化状态等均匀分散在某一固态载体中的体系。一般颗粒粒度大于100 µm,属于颗粒剂的范畴。包埋(缓释)颗粒剂的载体采用具有缓释性能的高分子聚合物,制备原理为固体分散技术,以区别于常规颗粒剂采用的载体为矿物性无机材料,及简单的机械混合与捏合。
2.1 包埋(缓释)颗粒剂与常规颗粒剂的比较
包埋(缓释)颗粒剂制备利用固体分散技术原理,与常规颗粒剂的机械物理混合制备具有云泥之别。与常规颗粒剂比较,具有以下显著的差异。
2.1.1 制备方法不同
常规颗粒剂的制备方法是以矿物性无机填料(如高岭土、黏土、硅藻土、碳酸钙等)与农药有效成分进行简单的机械粉碎、混合、捏合、造粒、干燥、筛分等加工工序制备,由于载体不具有缓释作用,其产品也没有缓释作用。另一类吸附性的载体如白炭黑等能够吸附农药有效成分,其制备的颗粒剂具有一定的缓释作用。为了使这类载体具有更强的吸附性能,需要粉碎为很细小的颗粒(一般在100 µm以下),使之具有更大的比表面积,吸附更多的农药有效成分,这样形成的颗粒小于常规颗粒剂的范畴,但由于颗粒小,容易释放,削弱了其缓释性能,无法达到实际需求的缓释性能。
包埋(缓释)颗粒剂是一类具缓释性能的农药新剂型,即利用固体分散技术,通过加热使低熔点高分子聚合物载体处于熔融状态,使农药有效成分与熔融态的载体混合均匀或在熔融态的载体中熔解,形成固态溶液,经过冷却、粉碎、筛分,形成一定粒径范围的粒状剂型。该颗粒剂中的有效成分以分子状态包埋在高分子聚合物中形成均匀颗粒,亦称为放大的微球(对应于微米级的微球剂)。包埋(缓释)颗粒剂也可采用复凝聚法制备,农药有效成分在高分子聚合物载体中形成均相乳状液,在交联剂的作用下,包含农药有效成分和高分子聚合物载体的乳状液凝聚成球,从水相中分离出来,经过干燥、粉碎、筛分,形成一定粒径范围的粒状剂型。包埋(缓释)颗粒剂外观与常规颗粒剂无异。
包埋(缓释)颗粒剂采用的载体是高分子聚合物,本身具有很强的缓释作用,因而该剂型也具有缓释性能。
2.1.2 释放机理不同
常规颗粒剂进行撒施使用,在土壤中水分的作用下很快崩解,农药有效成分完全释放出来,虽然具有一定的持效期(相对于叶面喷雾的农药剂型),但达不到缓释剂型的持效期。而包埋(缓释)颗粒剂中的农药有效成分是与具有缓释性能的载体均匀包埋,载体在土壤微生物的作用下缓慢降解,其农药有效成分随之释放出来。包埋(缓释)颗粒剂释放机理与微球剂类似,在施药初期,分布在包埋(缓释)颗粒剂表面的少量有效成分直接扩散到环境中,是导致施药初期突释的主要原因,也是包埋(缓释)颗粒剂具有一定速效的原因。包埋(缓释)颗粒剂进入土壤中,载体因吸水产生溶胀,包埋(缓释)颗粒剂的孔隙变大,内部的农药有效成分会通过溶胀后产生的孔道扩散到环境中,使包埋(缓释)颗粒剂发挥缓释作用。有效成分随着载体的降解同期释放是包埋(缓释)颗粒剂释放的主要方式,载体在环境中通过水解、微生物降解等途径逐渐分解,包埋在载体内部的有效成分被缓慢释放出来,发挥药效后随即在环境中完全降解,无农药残留风险。
2.1.3 施药方法的差异
常规颗粒剂的农药有效成分质量分数一般较低,大多低于5%,所以在土壤中进行撒施或跟肥料混合进行撒施。而包埋(缓释)颗粒剂由于载体的价格较昂贵,一般加工成较高质量分数的产品,如中国农业科学院植物保护研究所研制的噻虫胺包埋(缓释)颗粒剂的质量分数达到18%,采取定向(靶向)施用,与播种或幼苗移栽同时进行,一般采用穴施(蔬菜)或根施(果树),农药利用率明显高于撒施施药。
2.2 包埋(缓释)颗粒剂的应用实例
固体分散技术早期在农药中主要用于制备均一体,主要以塑料或橡胶为载体,制备各种形状具有缓释作用的固体均一体,以及采用β-环糊精为载体,制备包合物。最新的研究进展是采用具有缓释性能的高分子聚合物制备包埋(缓释)颗粒剂。
2.2.1 噻虫胺包埋(缓释)颗粒剂
噻虫胺包埋(缓释)颗粒剂的制备方法为熔融法。熔融法形成的固态溶液,可以在较低温度下熔化高熔点的有效成分(相当于有机溶剂在室温下溶解高熔点的农药有效成分),使之在大幅低于有效成分熔点的温度下制备 [如噻虫胺的熔点为176.8℃,而在载体的熔化温度下(70~80℃)即可与噻虫胺原药形成均匀的固态溶液]。一般以熔融法制备的载体均为低熔点(≤100℃)的天然高分子聚合物,如蜡质类、单硬脂酸甘油酯类、聚己内酯多元醇类、聚乙二醇类等,利用其可与高熔点的农药有效成分形成固态溶液的特性,即在较低的温度下农药有效成分可熔解于熔融状态的载体中,经过冷却、粉碎、筛分得到产品。
多元混合固体载体可以兼顾有效成分在载体中的熔解及均匀分散,提高固体分散体的持效性。中国农业科学院植物保护研究所研制的18%噻虫胺包埋(缓释)颗粒剂利用巴西棕榈蜡与聚乙二醇作为复合载体,在熔融状态下,利用亲水性的聚乙二醇熔解噻虫胺,再加入难溶性的巴西棕榈蜡形成固态溶液,经过冷却、粉碎、筛分获得产品。噻虫胺与聚乙二醇8000分子大小差异很大,噻虫胺分子只能填充进入聚乙二醇8000的晶格结构的空隙中形成填充型固态溶液,形成部分互熔的固态溶液,两者之间只能以一定的比例互熔。从X光射线衍射图谱可以看出,噻虫胺的衍射峰在制剂里面都能找到对应的峰,推断噻虫胺是以微晶态包埋在载体材料中(图3)。
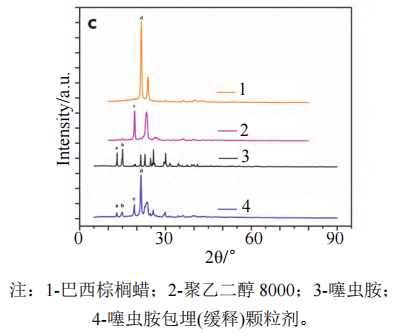
图3 噻虫胺包埋(缓释)颗粒剂X射线衍射分析
18%噻虫胺包埋(缓释)颗粒剂粒径为150~250μm,包埋率达到93%以上。该剂对花生蛴螬的持效期可长达4个月以上,处理后的虫口减退率高达83.2%,于花生收获前调查,处理蛴螬虫口密度降至(1.27±0.34)头/m2,低于花生田蛴螬2头/m2的防治指标。噻虫胺包埋(缓释)颗粒剂在花生中无残留风险 [花生仁的平均残留量为(3.76±1.02)µg/kg,大大低于水稻糙米上的残留标准<200 µg/kg;花生壳的平均残留量为(453.2±41.74)µg/kg,也低于水稻稻谷的残留标准<500 µg/kg,由于还没有噻虫胺在花生中的残留标准,以水稻的残留标准作为参考],可以安全使用。
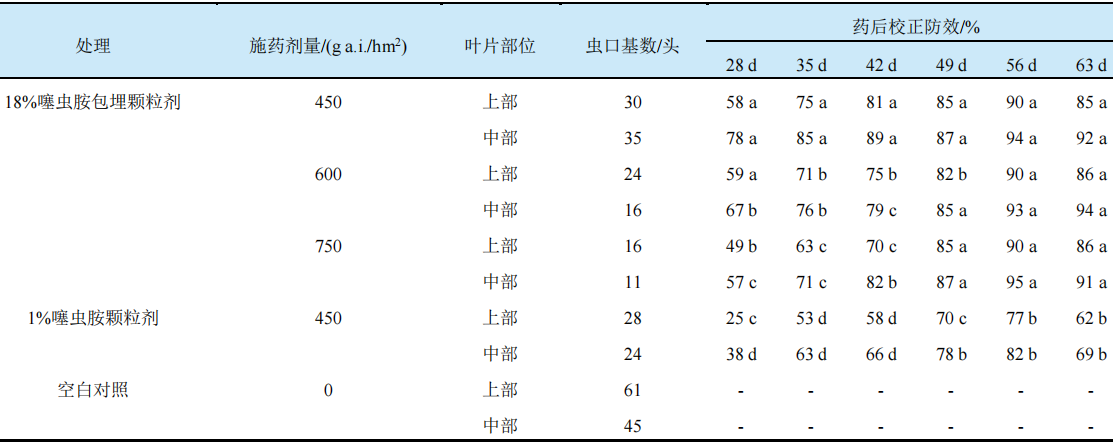
田间药效试验结果表明,噻虫胺包埋(缓释)颗粒剂对柑橘木虱的持效期可长达3个月以上,药后96 d同等剂量下比对照的防效高25%(表1)。对温室黄瓜白粉虱的持效期可达到2个月以上,药后63d同等剂量下噻虫胺包埋(缓释)颗粒剂对黄瓜白粉虱的防效仍在85%以上,比对照防效高20%以上(表2)。
表1 噻虫胺包埋(缓释)颗粒剂对柑橘(幼树)木虱的田间药效(湖南江华,2018年)
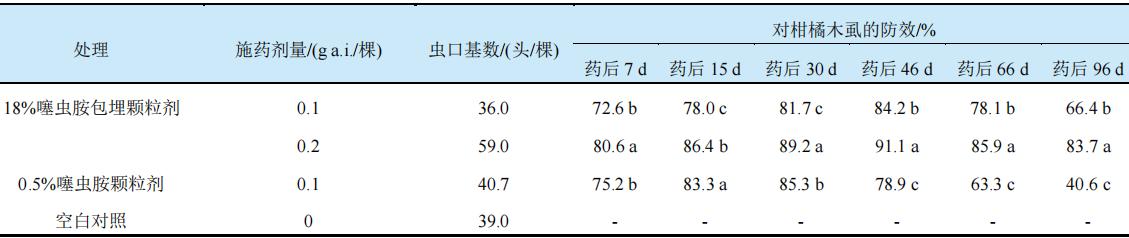
表2 噻虫胺包埋(缓释)颗粒剂对温室黄瓜白粉虱的防效(植保所温室,2019年)
噻虫胺包埋(缓释)颗粒剂对非靶标生物的安全性评价试验表明,其对蜜蜂的急性毒性仅为对照颗粒剂毒性的1/115,对家蚕的急性毒性仅为对照颗粒剂毒性的1/104,表明对非靶标生物具一定的安全性。
2.2.2 阿维菌素B2包埋(缓释)颗粒剂
中国农业科学院植物保护研究所以壳聚糖与海藻酸钠为复合载体采用复凝聚法成功制备了阿维菌素B2包埋(缓释)颗粒剂。海藻酸钠溶于水带负电,壳聚糖溶于弱酸性溶液带正电,2者是复凝聚制备方法中常见的载体组合,这2种高分子聚合物均为生物可降解的载体,对环境友好。利用壳聚糖的络合作用可改善海藻酸盐水凝胶的致密度,不仅有利于强化对有效成分的缓释作用,而且有助于改善海藻酸盐在碱性条件下的稳定性,防止其溶解,同时,壳聚糖自身在酸性条件下的稳定性也得到改善。此外,在壳聚糖中引入海藻酸钠也可以降低生产成本(海藻酸钠价格远低于壳聚糖)。
将阿维菌素B2溶于有机溶剂中,加入乳化剂混合均匀为油相,将油相缓慢加入海藻酸钠水溶液中,使用磁力搅拌器搅拌乳化。然后将乳液吸入注射器中,使用微量进样泵将乳液滴加至交联相中,交联相由壳聚糖、氯化钙水溶液组成。滴加完毕后再交联一定的时间,过滤,将其置于烘箱中干燥,再经过粉碎、筛分(60~100目的标准筛),成功制备外观不规则,无定形的22%阿维菌素B2包埋(缓释)颗粒剂。颗粒表面附着的有效成分含量为8%,粒径为150~300μm,包埋率为95%以上。包埋(缓释)颗粒剂在土壤中的模拟释放符合一级动力学方程及Higuchi方程,在土壤中80d的累积释放率为74.7%(土壤含水量15%以上,土壤温度20℃以上)。
3 利用固体分散技术制备的农药新剂型——微球剂
大多数农药微球剂的制备方法也是利用固体分散技术制备,只不过其外观为球形颗粒,粒径为微米级。
3.1 阿维菌素B2壳聚糖微球剂
针对阿维菌素类有效成分见光易分解,在土壤中易被土壤吸附,导致持效期大幅度缩短的缺点,研制了土壤根部施药的阿维菌素B2壳聚糖微球剂。此剂型是将农药有效成分包埋在高分子聚合物载体中,避免了有效成分与土壤的直接接触,不但延长了农药有效成分的持效期,而且改善了阿维菌素类农药有效成分在土壤施用易于被土壤吸附的缺陷。
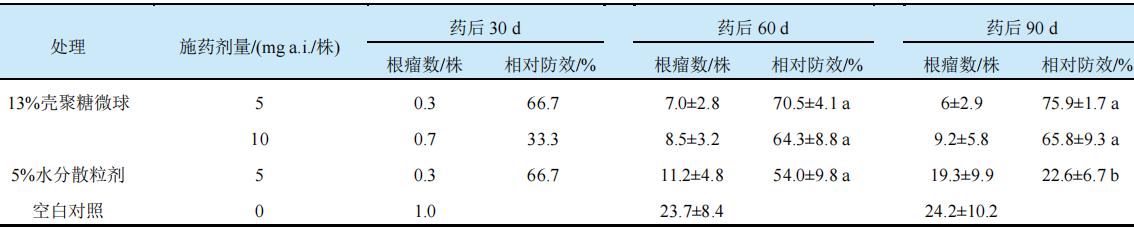
阿维菌素B2原药辅以少量有机溶剂及表面活性剂,在壳聚糖弱酸水溶液中搅拌形成乳状液,经喷雾干燥机喷雾,即可制备出实心的、形貌规则、粒径均匀的13%阿维菌素B2壳聚糖微球剂,粒径D50为10.7μm,D90为46.6μm,包埋率达到85%以上。由于采用喷雾干燥,在微球颗粒表面吸附了约占总载药量1/3的有效成分,因而兼具一定的速效性。在土壤中60 d释放75.7%的有效成分(土壤温度30℃,土壤含水量20%),在合适的条件下(土壤含水量15%以上,土壤温度20℃以上)具有优异的持效性。2016年在河北高邑县进行的防治黄瓜根结线虫病田间药效试验发现,同等剂量下(5 mg a.i./株),药后30 d,与对照药剂(5%阿维菌素B2水分散粒剂)防效相当,达到66.7%;药后60 d的防效为70.5%;药后90 d微球剂的防效为75.9%(对照药剂仅为22.6%),显著高于对照药剂(表3)。以上结果表明13%阿维菌素B2壳聚糖微球剂不仅速效性与对照药剂相媲美,且持效期显著高于对照药剂,持效期达到3个月以上,比对照药剂延长1个月。
表3 阿维菌素B2壳聚糖微球剂防治黄瓜根结线虫的田间药效试验(河北高邑,2016年)
3.2 噻虫胺壳聚糖微球剂
由于噻虫胺对蜜蜂及家蚕等经济昆虫高毒,叶面喷雾对这些有益经济昆虫影响大,研制了土壤根部施药的噻虫胺壳聚糖微球剂,避免烟碱类农药有效成分叶面喷雾对桑蚕的高毒问题,降低对桑蚕养殖业的影响,避开花期施药,减少对蜜蜂的影响。
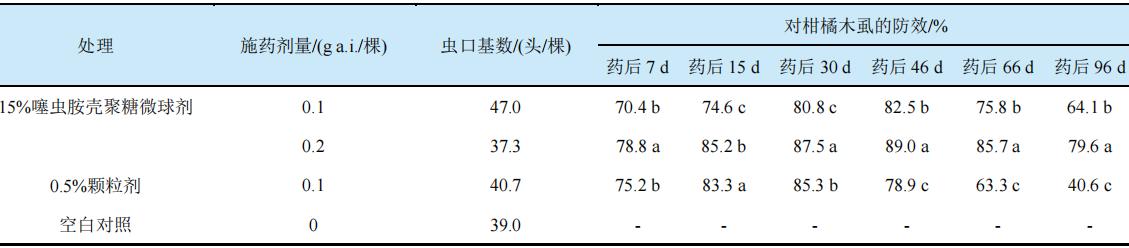
噻虫胺在加热搅拌条件下溶解于壳聚糖稀酸水溶液中,经喷雾干燥机喷雾,即可制备出实心的、形貌规则、粒径均匀的15%噻虫胺壳聚糖微球剂,D50为3.8μm,D90为10.4μm,微球剂表面附着的有效成分含量占总载药量的比例低于30%,包埋率达到96.8%,在土壤中60d的累积释放69.7%(土壤含水量15%,土壤温度30℃)。2018年在湖南江华防治柑橘木虱的药效试验表明,同等剂量下(幼树0.1 g a.i./棵),药后7 d与对照药剂(0.5%噻虫胺颗粒剂)防效相当,达到70.4%;药后46 d,防效为82.5%;药后96 d,防效为64.1%,而对照仅为40.6%,差异显著,即15%噻虫胺壳聚糖微球的速效性稍低于对照药剂,而持效期比对照药剂延长1个月以上(15%噻虫胺壳聚糖微球剂为3个月以上,而对照颗粒剂仅为2个月)(表4)。
表4 噻虫胺壳聚糖微球剂对柑橘木虱的田间药效(湖南江华,2018年)
对噻虫胺壳聚糖微球剂进行残留消解动态研究发现,15%噻虫胺壳聚糖微球剂在土壤中的消解半衰期比噻虫胺颗粒剂延长了15 d,微球剂的施用剂量提高1/3~2/3,其半衰期可延长28 d(表5)。15%噻虫胺壳聚糖微球剂对温室黄瓜白粉虱的防效施药后56 d达到高峰,施药后63d的防效比对照颗粒剂高18%以上(表6)。黄瓜叶片中吸收的噻虫胺累积量与防效呈正相关(相关系数约0.9,图4)。
表5 噻虫胺壳聚糖微球剂的残留消解动态
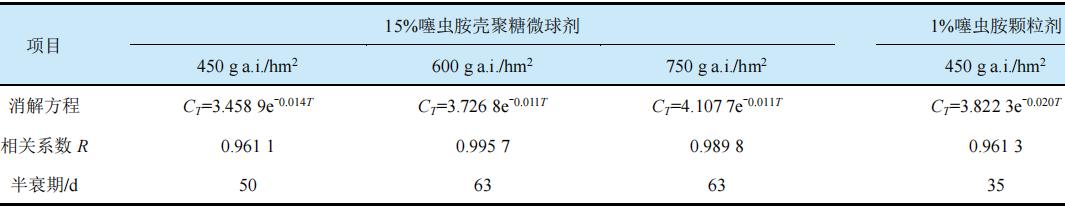
表6 噻虫胺壳聚糖微球剂对温室黄瓜白粉虱的防效(植保所温室,2019年)
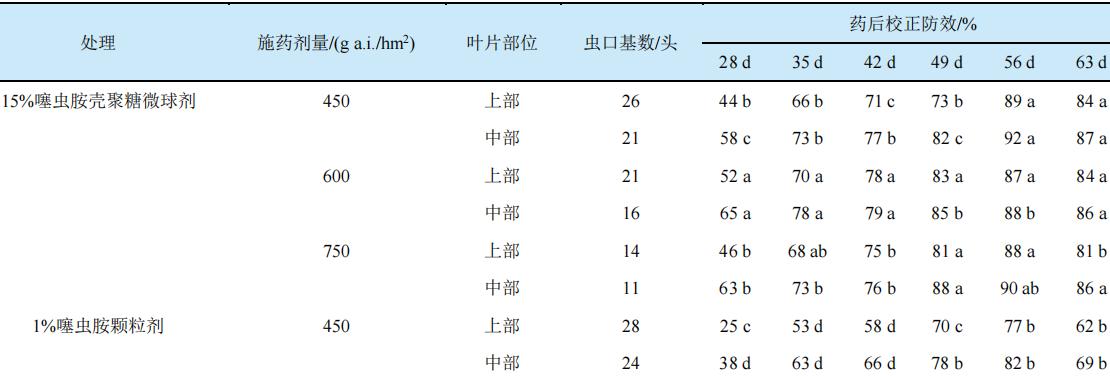

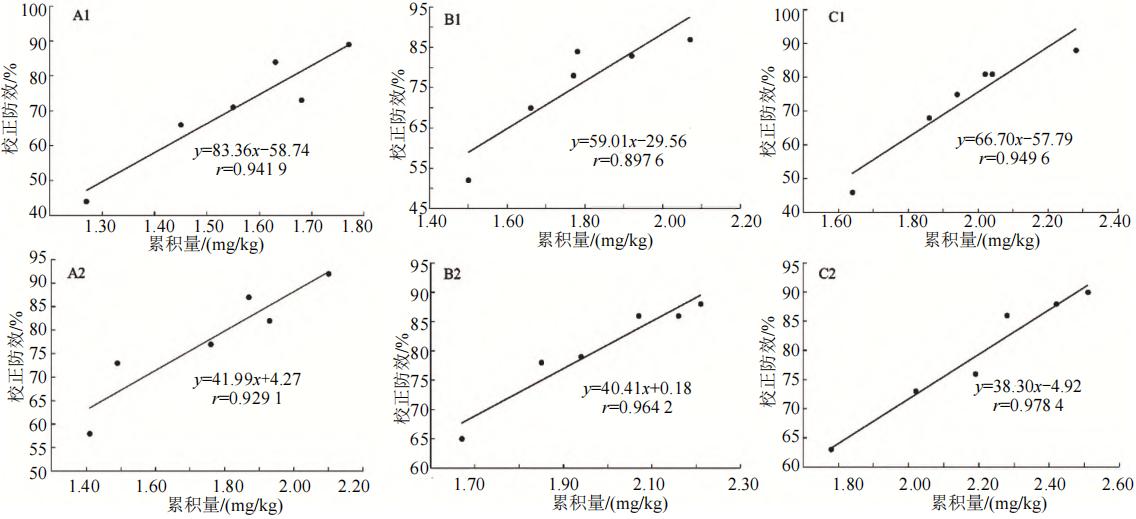
注:A、B、C分别为15%噻虫胺壳聚糖微球剂450、600、750 g a.i./hm2的施药剂量处理
图4 黄瓜上、中部叶片中噻虫胺累积量与噻虫胺壳聚糖微球剂对温室黄瓜白粉虱防效的相关性
3.3 呋虫胺壳聚糖/明胶微球剂
由于载体材料的不同,喷雾干燥法得到的微球剂结构不同,可分为中空微球及实心微球。农药有效成分与载体均匀包埋,形成的实心球体为实心微球,如壳聚糖微球剂;而农药与载体均匀混合形成一个中空壳状结构为中空微球剂,如明胶微球剂,外观为坍缩的球形(图5)。呋虫胺明胶微球剂载药量20%,包埋率98%以上,媲美于常规剂型的农药利用率。该剂对棉蚜的防治效果明显优于对照的颗粒剂,药后30 d防效可达到83.6%(颗粒剂仅为46.3%);药后79 d呋虫胺明胶微球对棉蚜的防效达到95.7%(颗粒剂为83.0%);药后97 d呋虫胺明胶微球的防效达72.4%(颗粒剂此时基本上失去了防治作用,仅为15.5%),表明呋虫胺明胶微球剂对棉蚜不但具有良好的速效性,而且具有长达3个月以上的持效性。
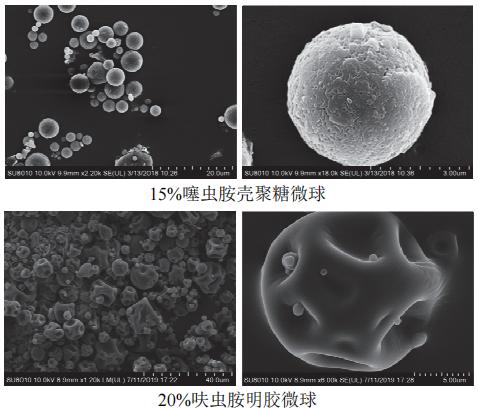
图5 壳聚糖微球(实心微球)与明胶微球(中空微球)的电镜照片
但由于明胶的熔点较低,热稳定性较差,需在明胶中引入其他的载体对其进行结构修饰,如引入壳聚糖对明胶微球进行修饰,当比例达到5∶1以上时,形成的微球剂外观为实心均匀的球形,且热稳定性明显提高。采用壳聚糖/明胶为1∶1制备的复合微球,载药量为18.5%,包埋率达到98%以上,微球剂粒径为8.6μm,跨度1.3,分布非常均匀。图6为呋虫胺壳聚糖/明胶微球剂的扫描电镜照片。
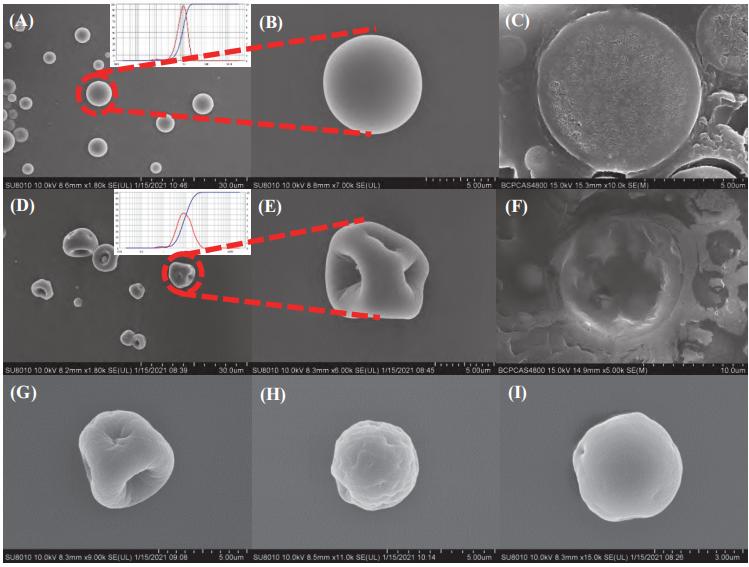
注:A、B、C为1∶1的壳聚糖/明胶微球,D、E、F为明胶微球,G、H、I为明胶与壳聚糖7∶1、5∶1、3∶1微球。
图6 呋虫胺壳聚糖/明胶微球剂的扫描电镜照片
对呋虫胺壳聚糖/明胶微球剂进行的土壤淋溶试验发现,微球剂最高比原药减少了46%的淋溶量,比颗粒剂减少20%的淋溶量,表明包覆在壳聚糖/明胶复合载体中的有效成分被固定在土壤中,从而减少极性农药的淋溶(图7)。
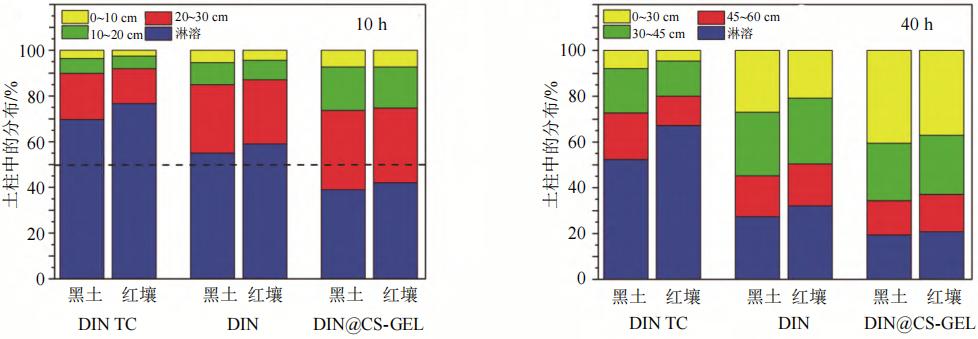
注:呋虫胺原药(DINTC);呋虫胺颗粒剂(DIN);呋虫胺壳聚糖/明胶微球剂(DIN@CS-GEL)
图7 呋虫胺壳聚糖/明胶微球剂的淋溶试验结果
对呋虫胺壳聚糖/明胶微球剂进行的残留消解动态研究表明,其在土壤中的半衰期比市售的颗粒剂(3%呋虫胺颗粒剂)延长了11 d(表7)。在施药后14~42d,市售颗粒剂在土壤中的消解率比呋虫胺壳聚糖/明胶微球剂高15.3%~35.2%,施药后35 d达到高峰。42 d呋虫胺壳聚糖/明胶微球剂在叶片中的呋虫胺累积量比市售颗粒剂高19.4%~22.8%(图8)。在施药后21~42 d,呋虫胺壳聚糖/明胶微球剂对白粉虱的防治效果比相同剂量的市售颗粒剂高16.9%~26.8%,施药后35 d药效达到高峰,42 d防效仍比对照药剂高18%以上(表8)。
表7 呋虫胺壳聚糖/明胶微球剂的残留消解动态
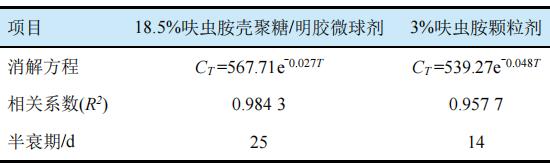

图8 呋虫胺壳聚糖/明胶微球剂在土壤及叶片中的残留消解动态
表8 呋虫胺壳聚糖/明胶微球剂对温室黄瓜白粉虱的防效(植保所温室,2021年) 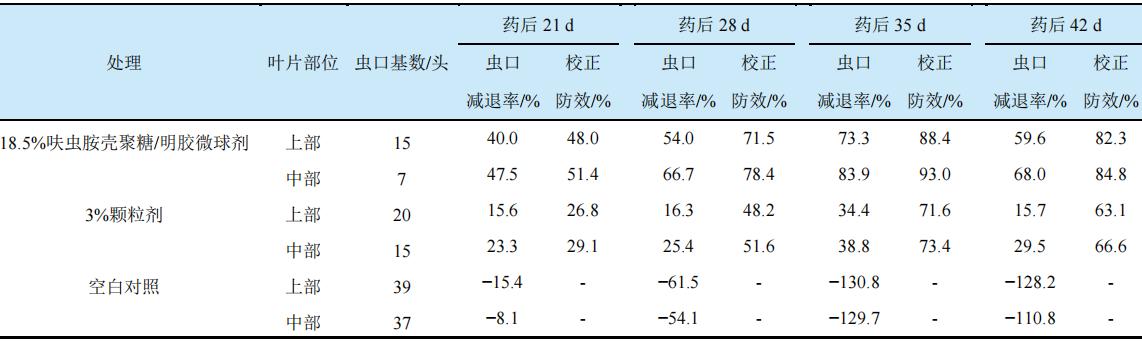
4 固体分散技术在农药制剂上应用展望
采用高分子聚合物载体制备缓释型固体分散体是固体分散技术在农药制剂上的成功应用范例,需要在农药制剂上不断完善,根据应用场景改善农药制剂的缓释性能,如根据不同的应用场景,针对不同应用场景的农药持效期的差异,设计出不同颗粒粒径、不同外观形状的固体分散体,生产出差异化的固体分散体。
利用固体分散体的靶向释放特点,可制备不同环境响应性的固体分散体。利用不同特性的载体,可设计出pH敏感型、温敏型、湿敏型、光敏型等的固体分散体。还可设计出具智能释放的农药固体分散体。
固体分散体配方简单,制备工艺简便,但毕竟属于农药制剂崭新的领域,需要农药制剂研发者与工艺设备开发者联合开发适合农药生产的固体分散体的工艺设备、工艺流程,为固体分散体在农药制剂的推广应用提供技术支撑及技术保障。
(1)本网旨在传播信息,促进交流,多方面了解农药发展动态,但不构成任何投资建议。
(2)所有文章仅代表作者观点,不代表本网立场。
(3)“信息来源:江苏省农药协会 农药资讯网”为原创文章,转载时请注明来源和作者。
(4)本网转载文章及图片的版权属于原作者,若有侵权,请联系删除。